Perbezaan antara pengaliran elektronik dan ionik
The Perbezaan utama antara pengaliran elektronik dan ionik ialah Pengaliran elektronik adalah pergerakan elektron dari satu tempat ke tempat lain, sedangkan pengaliran ionik adalah pergerakan ion dari satu tempat ke tempat lain.
Istilah pengaliran merujuk kepada pemindahan tenaga melalui bahan. Di sini, tenaga boleh dipindahkan dalam pelbagai bentuk seperti haba dan elektrik. Pengaliran elektronik dan pengaliran ionik adalah dua bentuk kaedah pemindahan tenaga yang dikategorikan berdasarkan medium pengaliran.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah pengaliran elektronik
3. Apakah pengaliran ionik
4. Perbandingan sampingan - pengaliran ionik vs elektronik dalam bentuk jadual
5. Ringkasan
Apakah pengaliran elektronik?
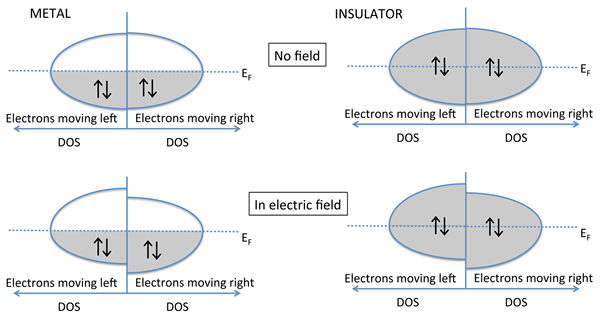
Pengaliran elektronik adalah proses memindahkan tenaga dalam bentuk arus elektrik. Di sini, kaedah pengaliran adalah pergerakan elektron. Walau bagaimanapun, mana -mana elektron dalam mana -mana sistem tidak dapat menyumbang kepada kaedah pengaliran ini. Elektron mesti berada di negeri bebas untuk bergerak dari satu tempat ke tempat lain. Elektron shell dalaman atom tidak dapat bergerak. Keperluan lain ialah kehadiran medan elektrik yang boleh menyebabkan pergerakan elektron bebas.

Rajah 01: Pengaliran elektron
Elektron yang dapat menjalani pengaliran dipanggil "elektron pengaliran". Elektron ini tidak dipasang dengan kuat pada mana -mana atom atau molekul. Elektron bebas ini boleh melompat dari orbital atom ke orbital atom bersebelahan. Walau bagaimanapun, secara keseluruhan, elektron ini terikat kepada konduktor. Pergerakan elektron bermula dengan penggunaan medan elektrik. Medan elektrik memberikan elektron arah untuk bergerak.
Apakah pengaliran ionik?
Pengaliran ionik adalah proses memindahkan tenaga melalui pergerakan spesies ionik. Semasa pengaliran ionik, spesies ionik yang berbeza bergerak dari satu tempat ke tempat lain mengikut kecerunan ionik. Ion adalah spesies yang dikenakan; ia boleh dikenakan secara positif atau dikenakan bayaran negatif. Ion yang dicas secara positif bergerak ke arah tempat yang dikenakan negatif dan sebaliknya. Kecenderungan bahan ke arah pengaliran ionik diukur sebagai kekonduksian ionik. Ia dilambangkan oleh λ.
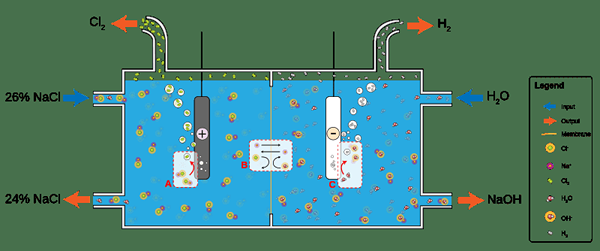
Rajah 02: Sel membran yang digunakan dalam elektrolisis larutan air garam di mana pengaliran ionik berlaku melalui membran di tengah untuk mengekalkan kepekatan ionik stabil.
Selalunya, kami menggunakan istilah pengaliran ionik mengenai kisi kristal. Di sini, pengaliran ionik merujuk kepada pergerakan ion dari satu kecacatan ke yang lain dalam kekisi kristal. Proses pengaliran ion adalah mekanisme arus di mana tenaga diluluskan dari satu tempat ke tempat lain.
Apakah perbezaan antara pengaliran elektronik dan ionik?
Pengaliran elektronik dan pengaliran ionik adalah dua bentuk kaedah pemindahan tenaga yang dikategorikan berdasarkan medium pengaliran. Perbezaan utama antara pengaliran elektronik dan ionik ialah pengaliran elektronik adalah pergerakan elektron dari satu tempat ke tempat lain, sedangkan pengaliran ionik adalah pergerakan ion dari satu tempat ke tempat lain.
Berikut adalah jadual ringkasan perbezaan antara pengaliran elektronik dan ionik.
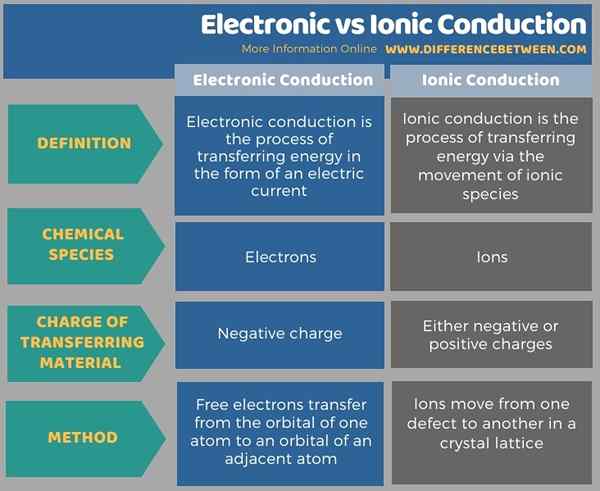
Ringkasan -Pengaliran ionik elektronik vs
Pengaliran elektronik dan pengaliran ionik adalah dua bentuk kaedah pemindahan tenaga yang dikategorikan berdasarkan medium pengaliran. Perbezaan utama antara pengaliran elektronik dan ionik ialah pengaliran elektronik adalah pergerakan elektron dari satu tempat ke tempat lain, sedangkan pengaliran ionik adalah pergerakan ion dari satu tempat ke tempat lain.
Rujukan:
1. "Pengaliran logam."Encyclopædia Britannica, Encyclopædia Britannica, Inc., Terdapat di sini.
2. "Pengaliran elektrik."ScienceDaily, ScienceDaily, boleh didapati di sini.
Ihsan gambar:
1. "Pengaliran E vs DOS" oleh TEM5Psu - Kerja Sendiri (CC BY -SA 4.0) melalui Commons Wikimedia
2. "Membran Chloralkali" oleh JKWCHUI - Berdasarkan * Bommaraju, Tilak V.; Orosz, Paul J.; Sokol, Elizabeth a.(2007). "Elektrolisis air garam."Ensiklopedia Elektrokimia. Cleveland: Case Western Rsserve University.MSN Encarta. "Elektrolisis Chloralkali."Diarkibkan 2009-10-31 (CC BY-SA 3.0) melalui Commons Wikimedia


