Perbezaan antara faktor pencairan dan pencairan

Perbezaan utama - Pencairan vs faktor pencairan
Faktor pencairan dan pencairan adalah istilah biasa yang digunakan untuk pengiraan dalam kimia analisis. Pencairan merujuk kepada penurunan kepekatan pelarut tertentu dalam penyelesaian. Istilah ini boleh digunakan untuk menggambarkan kedua -dua cecair dan gas. Faktor pencairan adalah ukuran pencairan; ia menerangkan sejauh mana pencairan. Perbezaan utama antara faktor pencairan dan pencairan ialah Pencairan penyelesaian adalah penurunan kepekatan larutan dalam penyelesaian itu manakala faktor pencairan adalah nisbah antara jumlah akhir dan jumlah awal penyelesaiannya.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu pencairan
3. Apakah faktor pencairan
4. Perbandingan sampingan -pencairan vs faktor pencairan dalam bentuk jadual
5. Ringkasan
Apa itu pencairan?
Pencairan penyelesaian adalah penurunan kepekatan larutan dalam penyelesaian itu. Penyelesaiannya terdiri daripada pelarut yang telah melarutkan larutan di dalamnya. Kepekatan larutan ini diberikan sebagai molariti atau molalitas. Molariti adalah jumlah larutan yang terdapat dalam jumlah penyelesaian unit (diberikan oleh unit mol/l). Molality adalah jisim larut yang hadir dalam jumlah unit (diberikan oleh unit kg/l). Apabila kepekatan larut dalam larutan ini berkurangan, ia dipanggil penyelesaian yang dicairkan.
Pencairan dilakukan dengan hanya menambahkan lebih banyak pelarut kepada penyelesaian, memegang kandungan larut yang tetap. Contohnya, larutan berair yang mengandungi natrium klorida (NaCl) boleh dicairkan dengan menambahkan lebih banyak air. Sekiranya larutan adalah sebatian berwarna, warna larutan memudar apabila penyelesaiannya dicairkan.

Rajah 1: Warna pudar apabila dicairkan
Pengiraan kepekatan akhir
Kepekatan akhir penyelesaian dapat ditentukan menggunakan hubungan berikut.
C1v1 = C2V2
C1 adalah kepekatan awal
V1 adalah jumlah awal
C2 adalah kepekatan akhir
V2 adalah jumlah akhir penyelesaiannya.
Ex: Penyelesaian berair KCl mengandungi 2.0 Moles of KCl dalam 0.2 L Air. Apa yang akan menjadi kepekatan akhir penyelesaian KCl jika air (400 ml) ditambah?
Kepekatan awal KCl (C1) = 2.0 mol/0.2L = 10 mol/l
Jumlah awal penyelesaian (v1) = 0.2 l
Jumlah akhir penyelesaian (v2) = 0.2 l + 0.4 L = 0.6 l
Kepekatan akhir penyelesaian (C2) boleh ditentukan menggunakan:
C1v1 = C2V2
10 mol/l x 0.2 L = C2 x 0.6 l
C2 = 2 mol / 0.6 L = 3.33 mol/l
Apakah faktor pencairan?
Faktor pencairan (juga dikenali sebagai nisbah pencairan) adalah nisbah antara jumlah akhir dan jumlah awal penyelesaian. Jumlah akhir adalah jumlah penyelesaian selepas pencairan. Jumlah awal adalah jumlah penyelesaian sebelum dicairkan, atau jumlah penyelesaian asal yang digunakan untuk pencairan. Hubungan ini juga boleh digunakan bersama dengan jisim larut.
Pengiraan faktor pencairan
Faktor Pencairan = Volume Akhir (V2) / Volume Awal (V1)
Contoh: pencairan 200 ml kmno4 penyelesaian berair dengan menambahkan 200ml air,
Faktor Pencairan = (200ml + 200ml) / 200ml
= 400 ml /200ml
= 2
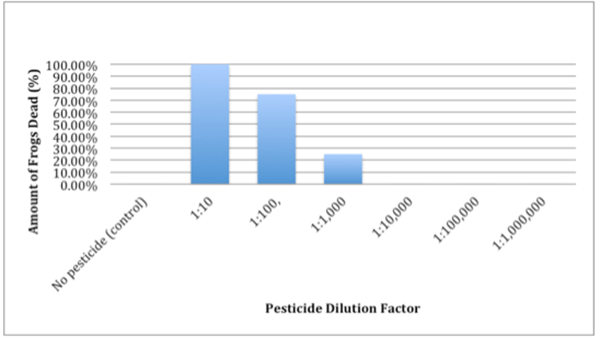
Rajah 02: Grafik faktor pencairan
Gambar rajah di atas menunjukkan graf dari penyelidikan di mana kematian katak dikira bersama dengan pencairan racun perosak yang ditambahkan ke ekosistem.
Apakah perbezaan antara faktor pencairan dan pencairan?
Pencairan vs faktor pencairan | |
| Pencairan penyelesaian adalah penurunan kepekatan larutan dalam penyelesaian itu. | Faktor Pencairan (Nisbah Pencairan) adalah nisbah antara jumlah akhir dan jumlah awal penyelesaiannya. |
| Konsep | |
| Pencairan adalah penurunan kepekatan. | Faktor pencairan adalah ukuran pencairan. |
| Keazaman | |
| Pencairan ditentukan oleh persamaan c1v1 = c2v2. | Faktor pencairan ditentukan dengan membahagikan jumlah akhir penyelesaian dari jumlah awal. |
| Unit | |
| Pencairan memberikan kepekatan akhir dalam unit mol/l. | Faktor pencairan tidak unit. |
Ringkasan -Pencairan vs faktor pencairan
Faktor pencairan dan pencairan adalah istilah yang sangat biasa dalam kimia. Faktor pencairan adalah ukuran pencairan. Perbezaan utama antara faktor pencairan dan pencairan ialah pencairan penyelesaian adalah penurunan kepekatan larutan dalam larutan itu manakala faktor pencairan adalah nisbah antara jumlah akhir dan jumlah awal penyelesaian.
Rujukan:
1. "Pencairan (Persamaan)."Wikipedia, Yayasan Wikimedia, 12 Feb. 2018, boleh didapati di sini.
2. "Pencahatan: Penjelasan dan Contohnya."Quansys Biosciences, tersedia di sini.
Ihsan gambar:
1. "Pencairan Penyebaran" oleh Tess Watson (CC oleh 2.0) melalui Flickr
2. "Rajah 1 Xenopus Laevis" oleh Krmeyer0717 - Kerja Sendiri (CC BY -SA 4.0) melalui Commons Wikimedia


