Perbezaan antara Deuteron dan Triton
The Perbezaan utama Antara Deuteron dan Triton ialah Deuteron adalah nukleus atom deuterium, sedangkan triton adalah nukleus atom tritium.
Hidrogen elemen kimia mempunyai tiga isotop utama. Mereka adalah protium, deuterium dan tritium. Ketiga isotop ini berbeza antara satu sama lain bergantung kepada bilangan neutron dalam nukleus mereka. Tritium mempunyai dua neutron dalam nukleusnya sementara deuterium hanya mempunyai satu neutron dalam nukleusnya.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu deuteron
3. Apa itu Triton
4. Perbandingan sampingan - Deuteron vs Triton dalam bentuk jadual
5. Ringkasan
Apa itu deuteron?
Deuteron adalah nukleus deuterium. Deuterium adalah isotop hidrogen yang mempunyai proton, neutron dan elektron. Tidak seperti Protium, isotop ini mempunyai proton dan neutron bersama dalam nukleus atom. Oleh itu, jisim atom isotop ini adalah 2. Itulah sebabnya kita boleh menamakannya sebagai hidrogen-2 atau 2H. Deuterium juga merupakan isotop stabil hidrogen. Walau bagaimanapun, ia tidak banyak berbanding protium. Kelimpahan berbeza antara 0.0026-0.0184%. Tidak seperti tritium, deuterium tidak radioaktif. Ia juga tidak menunjukkan ketoksikan.

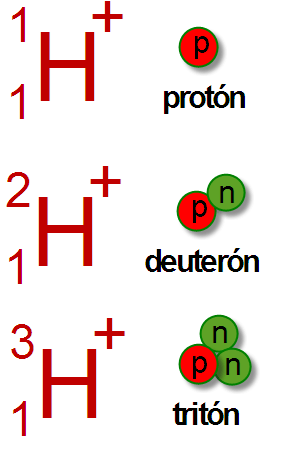
Rajah 01: isotop hidrogen yang berbeza; Nama nukleus isotop hidrogen
Air biasanya mengandungi hidrogen-1 yang digabungkan dengan atom oksigen. Tetapi, air juga boleh terbentuk dengan gabungan hidrogen-2 dan oksigen. Ini adalah air berat. Formula kimia untuk air berat adalah d2O di mana d adalah deuterium dan o adalah oksigen. Selain itu, kita boleh menggunakan deuterium dan sebatiannya dalam eksperimen kimia. Sebagai contoh, mereka berguna sebagai label bukan radioaktif dalam eksperimen seperti pelarut yang digunakan dalam spektroskopi NMR. Di samping itu, kita boleh menggunakan air berat sebagai moderator neutron dan penyejuk untuk reaktor nuklear. Deuterium juga merupakan bahan bakar untuk pembelahan nuklear yang dijalankan dalam skala komersial.
Apa itu Triton
Triton adalah nukleus tritium. Tritium adalah isotop hidrogen yang nombor jisimnya adalah tiga. Oleh itu, nukleus tritium mempunyai satu proton dan dua neutron. Ia hanya wujud dalam jumlah jejak kerana radioaktiviti. Kerana sebab ini, ia harus dihasilkan secara buatan untuk penggunaan praktikal.
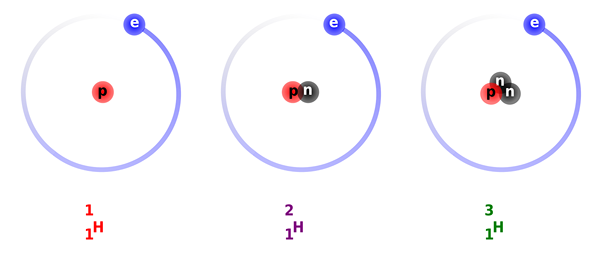
Rajah 02: Isotop hidrogen
Tritium adalah isotop radioaktif (ini adalah satu -satunya isotop radioaktif hidrogen). Ia mempunyai separuh hayat 12 tahun, dan ia merosot dengan memancarkan zarah beta untuk menghasilkan helium-3. Jisim atom isotop ini adalah 3.0160492. Selain itu, ia wujud sebagai gas (HT) pada suhu dan tekanan standard. Ia juga boleh membentuk oksida (HTO), yang kita panggil "air tritiated."Tritium berguna dalam membuat senjata nuklear dan sebagai pengesan dalam kajian biologi dan alam sekitar.
Apakah perbezaan antara Deuteron dan Triton?
Perbezaan utama antara Deuteron dan Triton ialah deuteron adalah nukleus deuterium, sedangkan Triton adalah nukleus tritium. Dalam hal ini, deuterium dan tritium adalah dua daripada tiga isotop hidrogen.
Lebih-lebih lagi, perbezaan lain antara Deuteron dan Triton ialah Deuteron bukan radioaktif manakala Triton adalah radioaktif. Juga, deuteron mempunyai dua komponen (proton dan neutron), manakala Triton mempunyai tiga komponen (proton dan dua neutron).

Ringkasan -Deuteron vs Triton
Hidrogen mempunyai tiga isotop utama: Protium, Deuterium dan Tritium. Ketiga isotop ini berbeza antara satu sama lain bergantung kepada bilangan neutron dalam nukleus mereka. Perbezaan utama antara Deuteron dan Triton ialah deuteron adalah nukleus deuterium, sedangkan Triton adalah nukleus tritium.
Rujukan:
1. Helmenstine, Anne Marie. "Fakta deuterium."Thoughtco, Feb. 11, 2020, boleh didapati di sini.
2. Helmenstine, Anne Marie. "10 fakta menarik mengenai tritium radioaktif."Thoughtco, Feb. 11, 2020, boleh didapati di sini.
Ihsan gambar:
1. "Hidron-Hydron" oleh Armando-Martin-Kerja Sendiri (CC BY-SA 4.0) melalui Commons Wikimedia
2. "Skema Nukleus Deuterium Tritium Hidrogen" oleh Kerja Derivatif: Uvainio (Talk) (CC BY-SA 3.0) melalui Commons Wikimedia


