Perbezaan antara borazine dan benzena
The Perbezaan utama antara borazine dan benzena ialah Borazine mengandungi tiga atom boron dan tiga atom nitrogen dalam struktur cincin manakala benzena mengandungi enam atom karbon dalam struktur cincin.
Kedua-dua borazine dan benzena mempunyai struktur yang sama dengan cincin enam anggota, dan kedua-dua sebatian ini adalah isoelektronik. Maksudnya, kedua -dua borazine dan benzena mempunyai bilangan elektron yang sama atau struktur elektronik yang sama. Walau bagaimanapun, mereka mempunyai sifat kimia dan fizikal yang sama sekali berbeza kerana cincin sebatian ini terdiri daripada atom yang berbeza.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu Borazine
3. Apa itu benzena
4. Persamaan antara borazine dan benzena
5. Perbandingan sampingan - borazine vs benzena dalam bentuk jadual
6. Ringkasan
Apa itu Borazine?
Borazine adalah sebatian bukan organik yang mempunyai formula kimia b3H6N3. Ia adalah sebatian kitaran dengan struktur cincin enam anggota. Iaitu, ia mempunyai tiga unit B-H dan tiga unit N-H dalam corak seli. Oleh itu, kita boleh menulis formula kimianya sebagai (BH3) (Nh3). Juga, struktur ini isoelektronik dengan cincin benzena. Seperti benzena, ini juga adalah cecair tanpa warna pada suhu bilik. Oleh itu, kita kadang -kadang menamakannya sebagai "benzena bukan organik".
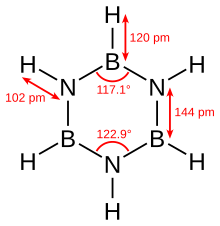
Rajah 01: Struktur kimia borazin
Tambahan pula, jisim molar borazine adalah 80.50 g/mol. Titik lebur dan titik mendidih masing -masing adalah -58 ° C dan 53 ° C. Juga, ia mempunyai bau aromatik. Selain itu, ini adalah sebatian sintetik yang dapat kita hasilkan dari diborane dan ammonia pada nisbah 1: 2.
Reaksi kimia yang terlibat dalam proses ini adalah seperti berikut:
3 b2H6 + 6 nh3 → 2 b3H6N3 + 12 jam2
Di atas semua, jika kita menambah borazine ke air, ia akan menghidrolisis untuk memberikan asid borik, ammonia dan gas hidrogen. Selain itu, sebatian ini sangat stabil kerana perubahan entalpi standard yang rendah; -531 kJ/mol. Juga, berbanding dengan benzena, borazine jauh lebih reaktif. Sebagai contoh, ia boleh bertindak balas dengan hidrogen klorida manakala benzena tidak boleh.
Menurut penentuan kristalografi sinar-X, panjang ikatan dalam struktur cincin borazine adalah sama. Walau bagaimanapun, ia tidak dapat membentuk segi enam yang sempurna kerana corak nitrogen dan boron yang berselang -seli memberikan sudut ikatan yang berbeza dan oleh itu, simetri molekul yang berbeza.
Apa itu benzena?
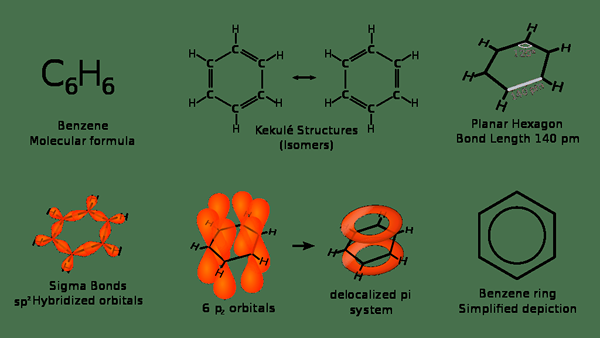
Benzene adalah sebatian organik yang mempunyai formula kimia c6H6. Ia mempunyai struktur cincin enam anggota dengan semua ahli adalah atom karbon. Di sini, setiap atom karbon ini dilampirkan pada atom hidrogen. Oleh kerana sebatian ini hanya mengandungi atom karbon dan hidrogen, ia adalah hidrokarbon. Di atas semua, kompaun ini secara semula jadi berlaku sebagai penyusun minyak mentah.

Rajah 02: Pelbagai representasi benzena
Melihat sifat mereka, jisim molar benzena adalah 78.11 g/mol. Titik lebur dan titik mendidih adalah 5.53 ° C dan 80.1 ° C. Juga, ia adalah cecair tidak berwarna pada suhu bilik. Tambahan pula, ia adalah hidrokarbon aromatik. Akibatnya, ia mempunyai bau aromatik. Selain itu, menurut penentuan difraksi sinar-X, semua ikatan antara enam atom karbon mempunyai panjang yang sama. Oleh itu, ia mempunyai struktur pertengahan. Kami menyebutnya sebagai "struktur hibrid" kerana menurut pembentukan bon, harus ada ikatan tunggal dan ikatan berganda antara atom karbon. Selanjutnya, struktur benzena sebenar adalah hasil daripada beberapa struktur resonans molekul benzena.
Apakah persamaan antara borazine dan benzena?
- Kedua -duanya adalah struktur kitaran.
- Juga, kedua-duanya, borazine dan benzena, mempunyai cincin enam anggota.
- Selain itu, kedua -duanya mempunyai panjang ikatan yang sama antara atom cincin.
- Tambahan pula, kedua -duanya adalah cecair tidak berwarna pada suhu bilik.
- Kedua -duanya juga isoelektronik.
Apakah perbezaan antara borazine dan benzena?
Borazine adalah sebatian bukan organik yang mempunyai formula kimia b3H6N3 sedangkan benzena adalah sebatian organik yang mempunyai formula kimia c6H6. Oleh itu, perbezaan utama antara borazine dan benzena adalah bahawa borazine mengandungi tiga atom boron dan tiga atom nitrogen dalam struktur cincin manakala benzena mengandungi enam atom karbon dalam struktur cincin. Di Borazine, atom boron dan nitrogen berada dalam corak seli. Akibatnya, molekul borazine bukan heksagon yang sempurna, tetapi benzena hanya mempunyai atom karbon di gelanggang. Oleh itu, ia boleh membentuk segi enam yang sempurna. Oleh itu, kita boleh menganggap ini sebagai perbezaan lain antara Borazine dan Benzene.
Di atas semua, perbezaan yang signifikan antara borazine dan benzena adalah bahawa borazine adalah sebatian sintetik manakala benzena secara semulajadi berlaku dalam minyak mentah sebagai penyusun utama. Juga, kita dapat mengenal pasti perbezaan antara borazine dan benzena berdasarkan kereaktifan mereka juga. Secara perbandingan, borazine lebih reaktif daripada benzena.

Ringkasan -Borazine vs Benzene
Borazine dan benzena adalah isoelektronik; bermaksud bahawa mereka mempunyai bilangan elektron yang sama atau struktur elektronik yang sama. Tetapi, mereka adalah dua sebatian yang berbeza. Dan, perbezaan utama antara borazine dan benzena adalah bahawa borazine mengandungi tiga atom boron dan tiga atom nitrogen dalam struktur cincin manakala benzena mengandungi enam atom karbon dalam struktur cincin.
Rujukan:
1. MN2555 Ikuti. "Borazine- Struktur, Penyediaan dan Hartanah."LinkedIn Slideshare, 24 Nov. 2015. Terdapat di sini
2. "Benzene."Wikipedia, Yayasan Wikimedia, 27 Sept. 2018. Terdapat di sini
Ihsan gambar:
1."Borazine-Dimensions-2D" oleh HBF878-Kerja Sendiri, (CC0) melalui Commons Wikimedia
2."Perwakilan Benzene" oleh Vladsinger - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia


