Perbezaan antara berat atom dan jisim atom
The Perbezaan utama antara berat atom dan jisim atom adalah bahawa Berat atom adalah berat purata elemen, berkenaan dengan semua isotopnya dan kelimpahan relatifnya tetapi jisim atom adalah jisim atom tunggal.
Kebanyakan orang menggunakan istilah jisim atom dan berat atom secara bergantian. Walau bagaimanapun, mereka mempunyai makna yang berbeza, dan ia menyebabkan kesilapan yang ketara dalam pengiraan bahan pukal jika kita mengambil kedua -dua istilah ini sebagai satu.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Berapakah berat badan atom
3. Apakah jisim atom
4. Perbandingan sampingan - Berat atom vs jisim atom dalam bentuk jadual
5. Ringkasan
Berapakah berat badan atom?
Berat atom adalah berat purata elemen, berkenaan dengan semua isotopnya dan kelimpahan relatifnya. Kebanyakan masa, elemen kimia mempunyai isotop; isotop adalah bentuk yang berbeza dari elemen kimia yang sama. Isotop mempunyai bilangan proton yang sama (yang menjadikannya tergolong dalam elemen kimia yang sama) dan bilangan neutron yang berlainan dalam nukleus atom. Terdapat peratusan yang berbeza dari isotop yang berbeza yang berlaku di alam. Kita perlu mempertimbangkan jisim atom semua isotop dan peratusan mereka apabila mendapat berat atom elemen kimia. Di sana, kita dapat mengira jisim purata menggunakan jisim atom setiap isotop untuk mendapatkan berat atom. Berat atom yang kita lihat dalam jadual berkala dikira mengikut fenomena ini.
Kita boleh menggunakan dua langkah berikut untuk pengiraan ini;
- Pertama, tukar peratusan ke dalam nilai perpuluhan dengan membahagikannya dengan 100.
- Seterusnya, kalikan massa atom setiap isotop dari nilai perpuluhan dengan sewajarnya.
- Akhirnya, tambahkan jawapan bersama untuk mendapatkan jawapan terakhir.
Video 1: Mengira berat atom
Contoh: Katakan kita mempunyai 98% isotop C-12 dan 2% daripada isotop C-13. Marilah kita mengira berat atom karbon menggunakan massa atom isotop ini.
- Menukar nilai perpuluhan:
- Nilai perpuluhan untuk peratusan C-12 ialah 0.98 (diperoleh dengan membahagikan 98 dari 100).
- Nilai perpuluhan untuk peratusan C-13 ialah 0.02 (diperoleh dengan membahagikan 2 dari 100).
- Pendaraban massa atom setiap isotop dari nilai perpuluhan:
- 12 x 0.98 = 11.76
- 13 x 0.02 = 0.26
- Penambahan jawapan bersama untuk mendapatkan jawapan terakhir:
- 76 + 0.26 = 12.02
Akhirnya, kita boleh mendapatkan berat atom karbon elemen kimia sebagai 12.02 AMU (unit jisim atom). Selain itu, kita boleh menamakan istilah ini sebagai "jisim atom relatif" kerana ia adalah purata massa atom sebenar isotop.
Apakah jisim atom?
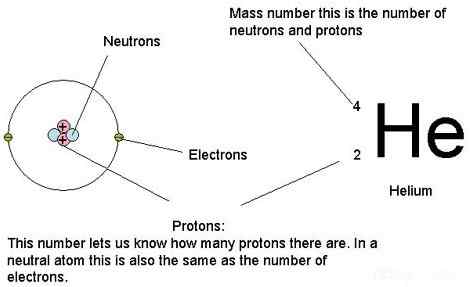
Atom terutamanya mengandungi proton, neutron dan elektron. Jisim atom hanyalah jisim atom. Dalam erti kata lain, ia adalah pengumpulan massa semua neutron, proton dan elektron dalam satu atom, khususnya, apabila atom tidak bergerak (jisim rehat). Kami hanya mengambil jisim yang lain kerana mengikut asas -asas fizik ketika atom bergerak pada halaju yang sangat tinggi, massa meningkat. Walau bagaimanapun, jisim elektron sangat kecil berbanding dengan massa proton dan neutron. Oleh itu, kita boleh mengatakan bahawa sumbangan elektron kepada jisim atom adalah kurang. Oleh itu kita boleh mengabaikan jisim elektron apabila mengira jisim atom. Di atas semua, isotop yang berbeza mempunyai massa atom yang berbeza walaupun mereka tergolong dalam elemen kimia yang sama kerana mereka mempunyai bilangan neutron yang berlainan.

Rajah 01: Kita boleh menggunakan massa proton, neutron dan elektron atom untuk mengira jisim atom
Selain itu, jisim atom sangat kecil, jadi kita tidak dapat menyatakannya dalam unit jisim normal seperti gram atau kilogram. Untuk tujuan kami, kami menggunakan unit jisim atom (AMU) unit lain untuk mengukur jisim atom. Begitu juga, 1 unit jisim atom adalah satu-dua belas jisim isotop C-12. Apabila kita membahagikan jisim atom dari jisim satu-dua belas jisim isotop C-12, kita boleh mendapatkan jisim relatifnya. Walau bagaimanapun, dalam penggunaan umum apabila kita mengatakan jisim atom relatif elemen, kita bermaksud berat atom mereka (kerana kita mengira ia memandangkan semua isotop).
Apakah perbezaan antara berat atom dan jisim atom?
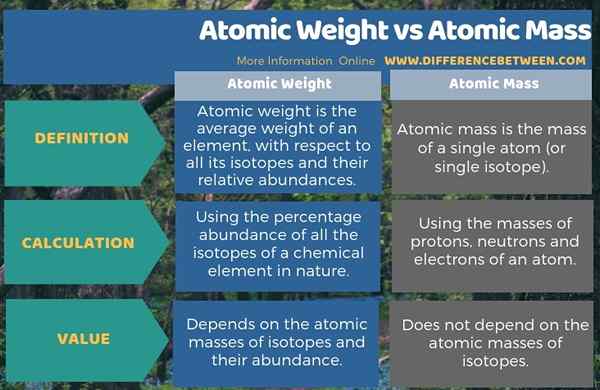
Kebanyakan masa kita menggunakan istilah berat atom dan jisim atom seperti yang sama. Walau bagaimanapun, kedua -dua istilah ini berbeza antara satu sama lain terutamanya mengikut definisi. Oleh itu, dengan definisi, perbezaan utama antara berat atom dan jisim atom adalah bahawa berat atom adalah berat purata unsur, berkenaan dengan semua isotopnya dan kelimpahan relatifnya sedangkan jisim atom adalah jisim satu atom tunggal.
Tambahan pula, kita dapat mengenal pasti satu lagi perbezaan penting antara berat atom dan jisim atom dengan mempertimbangkan cara mengira setiap nilai; Kita harus mengira berat atom menggunakan kelimpahan peratusan semua isotop unsur kimia dalam alam semula jadi sementara kita dapat mengira jisim atom hanya dengan menambahkan massa proton, neutron dan elektron atom.
Ringkasan -Berat atom vs jisim atom
Berat atom dan jisim atom adalah dua istilah penting yang sering kita gunakan dalam pengiraan kimia. Perbezaan utama antara berat atom dan jisim atom adalah bahawa berat atom adalah berat purata unsur, berkenaan dengan semua isotopnya dan kelimpahan relatifnya manakala jisim atom adalah jisim atom tunggal.
Rujukan:
1. Wichers, Edward, dan H. Steffen Peiser. "Berat atom."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 15 dec. 2017. Terdapat di sini
2. Helmenstine, Anne Marie, PH.D. "Cara mengira jisim atom."Thoughtco, APR. 1, 2018. Terdapat di sini
Ihsan gambar:
1."133317385" oleh eLearn.Punjab (CC0) melalui Vimeo
2."Penggambaran Nombor Atom" oleh MaterialScientist (CC0) melalui Commons Wikimedia


