Perbezaan antara aniline dan benzylamine
The Perbezaan utama antara aniline dan benzylamine adalah bahawa Kumpulan amina aniline dilampirkan pada cincin benzena secara langsung manakala kumpulan amina benzylamine dilampirkan pada cincin benzena secara tidak langsung, melalui A -ch2- kumpulan.
Aniline dan benzylamine adalah sebatian organik aromatik. Kedua -dua sebatian ini mengandungi cincin benzena dan kumpulan amina, tetapi kumpulan amina melampirkan benzena dengan cara yang berbeza; sama ada secara langsung atau tidak langsung. Oleh itu, kedua -dua sebatian mempunyai sifat kimia dan fizikal yang berbeza.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu Aniline
3. Apa itu benzylamine
4. Perbandingan sampingan - Aniline vs benzylamine dalam bentuk jadual
5. Ringkasan
Apa itu Aniline?
Aniline adalah sebatian organik aromatik yang mempunyai formula kimia c6H5NH2. Ia mempunyai kumpulan fenil (cincin benzena) dengan kumpulan amina yang dilampirkan (-NH2). Ia adalah amina aromatik yang paling mudah. Selain itu, sebatian ini sedikit piramidasi dan lebih rata daripada amina alifatik. Jisim molarnya adalah 93.13 g/mol. Titik lebur ialah -6.3 ° C sementara titik mendidih adalah 184.13 ° C. Ia mempunyai bau ikan busuk.
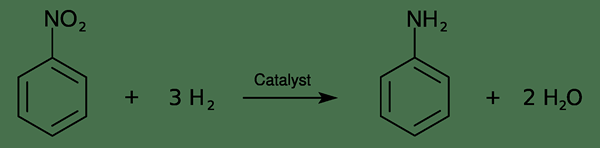
Secara industri, kita dapat menghasilkan sebatian ini melalui dua langkah. Langkah pertama ialah nitrasi benzena dengan campuran asid nitrik dan asid sulfurik (pada 50 hingga 60 ° C). Ia memberikan nitrobenzene. Kemudian, kita boleh menghidrogenasi nitrobenzene menjadi aniline dengan kehadiran pemangkin logam. Reaksi adalah seperti berikut;

Selain itu, sebatian ini digunakan terutamanya dalam pembuatan prekursor poliuretana. Selain itu, kita boleh menggunakan sebatian ini dalam pengeluaran pewarna, ubat -ubatan, bahan letupan, plastik, bahan kimia fotografi dan karet, dll.
Apa itu benzylamine?
Benzylamine adalah sebatian organik aromatik dengan formula kimia c6H5Ch2NH2. Ia mempunyai kumpulan amina yang melekat pada kumpulan fenil melalui kumpulan -ch2- kumpulan. Selain itu, sebatian ini berlaku sebagai cecair tanpa warna, dan ia mempunyai bau seperti ammonia. Jisim molar benzylamine adalah 107.15 g/mol. Titik lebur adalah 10 ° C manakala titik mendidih adalah 185 ° C.
Kita boleh menghasilkan kompaun ini melalui reaksi benzil klorida dengan ammonia. Juga, kita dapat menghasilkannya dengan pengurangan benzonitril. Reaksi adalah seperti berikut;
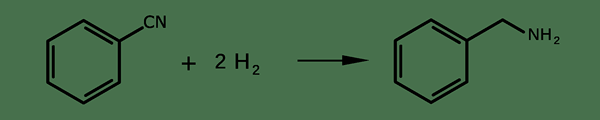
Selain itu, sebatian ini adalah pendahulu yang biasa untuk sintesis organik dan pengeluaran banyak farmaseutikal.
Apakah perbezaan antara aniline dan benzylamine?
Aniline adalah sebatian organik aromatik yang mempunyai formula kimia c6H5NH2 Walaupun benzylamine adalah sebatian organik aromatik yang mempunyai formula kimia c6H5Ch2NH2. Perbezaan utama antara aniline dan benzylamine ialah dalam aniline kumpulan amina melekat dengan cincin benzena secara langsung sedangkan dalam benzylamine kumpulan amina melekatkan cincin benzena secara tidak langsung, melalui kumpulan -ch2- kumpulan.
Selain itu, kita boleh menghasilkan aniline melalui nitrasi benzena diikuti dengan hidrogenasi nitrobenzene ke dalam aniline sedangkan kita dapat menghasilkan benzylamine melalui reaksi benzil klorida dengan ammonia. Selain itu, perbezaan selanjutnya antara aniline dan benzylamine adalah bau mereka. Aniline mempunyai bau ikan busuk sementara bau benzylamine serupa dengan bau ammonia.

Ringkasan -Aniline vs benzylamine
Aniline adalah sebatian organik aromatik yang mempunyai formula kimia c6H5NH2 Walaupun benzylamine adalah sebatian organik aromatik yang mempunyai formula kimia c6H5Ch2NH2. Ringkasnya, perbezaan utama antara aniline dan benzylamine adalah bahawa dalam aniline, kumpulan amina melekat dengan cincin benzena secara langsung sedangkan, dalam benzylamine, kumpulan amina melekatkan cincin benzena secara tidak langsung, melalui A -ch2- kumpulan.
Rujukan:
1. "Aniline."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 26 Sept. 2013, boleh didapati di sini.
Ihsan gambar:
1. "Aniline dari Nitrobenzene" oleh Hermann Luyken - Kerja Sendiri (CC0) melalui Commons Wikimedia
2. "Hidrogenasi Benzonitril" oleh Hermann Luyken - Kerja Sendiri (CC By -SA 3.0) melalui Commons Wikimedia


