Perbezaan antara konfigurasi gas mulia dan konfigurasi elektron
The Perbezaan utama Antara konfigurasi gas mulia dan konfigurasi elektron ialah a Konfigurasi gas mulia hanya mempunyai pasangan elektron manakala konfigurasi elektron boleh mempunyai elektron berpasangan dan tidak berpasangan.
Istilah konfigurasi elektron merujuk kepada urutan elektron atau susunan elektron yang terdapat dalam atom elemen kimia tertentu. Istilah konfigurasi elektron gas mulia menunjukkan bahawa semua orbital atom sepenuhnya diisi dengan elektron.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa konfigurasi gas mulia
3. Apakah konfigurasi elektron
4. Perbandingan sampingan - konfigurasi gas mulia vs konfigurasi elektron dalam bentuk jadual
5. Ringkasan
Apa konfigurasi gas mulia?
Konfigurasi Gas Noble adalah konfigurasi elektron atom gas mulia. Atom gas mulia adalah atom kumpulan 18 elemen kimia dalam jadual berkala. Kumpulan 18 elemen kimia dikenali sebagai unsur gas mulia kerana dua sebab; Pertama, unsur -unsur kimia ini kebanyakannya tidak aktif kerana konfigurasi elektron mereka yang lengkap, dan sebab kedua adalah bahawa unsur -unsur kimia ini berlaku dalam fasa gas.

Rajah 01: Gas mulia yang berbeza
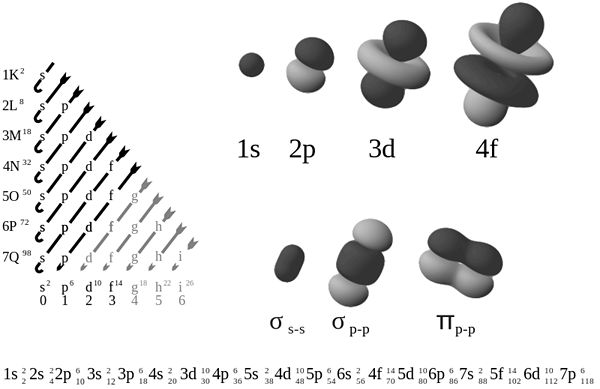
Terdapat empat jenis utama orbital atom dalam elemen kimia; s orbital, orbital p, orbital dan orbital f. Orbital atom S mengandungi maksimum dua elektron, orbital p boleh memegang enam elektron, orbital d boleh memegang sepuluh elektron, dan orbital f boleh memegang 14 elektron. Dalam kumpulan 18 elemen kimia, kita dapat melihat konfigurasi elektron S2P6; Di sini, orbital atom S dan P dipenuhi sepenuhnya dengan elektron. Oleh itu, tidak ada elektron yang tidak berpasangan di atom -atom ini.
Apakah konfigurasi elektron?
Konfigurasi elektron adalah pengagihan elektron atom dalam orbital atomnya. Istilah ini menerangkan setiap elektron dalam atom sebagai bergerak secara bebas dalam orbital, dalam bidang purata yang dibuat oleh semua orbital lain.
Konfigurasi elektron atom boleh dinyatakan sebagai urutan elektron yang terdapat dalam atom itu dalam bentuk pengedaran di seluruh orbital atom atom itu. Sesetengah elemen kimia seperti atom gas mulia telah menyelesaikan orbital atom, dan tidak ada elektron yang tidak berpasangan; Walau bagaimanapun, kebanyakan elemen kimia yang kita tahu mempunyai elektron yang tidak berpasangan dalam konfigurasi elektron mereka. Sebagai contoh, konfigurasi elektron atom neon, atom gas mulia, mempunyai konfigurasi elektron 1s22s22p6.

Dengan melihat konfigurasi elektron atom, kita dapat menggambarkan kereaktifan atom itu. Orbital atom yang sepenuhnya diisi menunjukkan sifat yang tidak aktif kerana ia tidak perlu mendapatkan lebih banyak elektron untuk menstabilkan dirinya sendiri. Sebaliknya, dalam atom yang mempunyai elektron yang tidak berpasangan sering cenderung sangat reaktif untuk menstabilkan konfigurasi elektron mereka.
Apakah perbezaan antara konfigurasi gas mulia dan konfigurasi elektron?
Konfigurasi gas mulia adalah konfigurasi elektron atom gas mulia; Ini bermakna, atom telah mengisi orbital atom sepenuhnya. Perbezaan utama antara konfigurasi gas mulia dan konfigurasi elektron adalah bahawa konfigurasi gas mulia hanya mempunyai pasangan elektron manakala konfigurasi elektron boleh mempunyai kedua -dua elektron berpasangan dan tidak berpasangan. Maksudnya; Konfigurasi gas mulia telah mengisi orbital atom sepenuhnya sementara konfigurasi elektron boleh sama ada diisi sepenuhnya atau orbital yang dipenuhi setengah.
Di bawah Infographic menyenaraikan lebih banyak perbezaan antara konfigurasi gas mulia dan konfigurasi elektron.
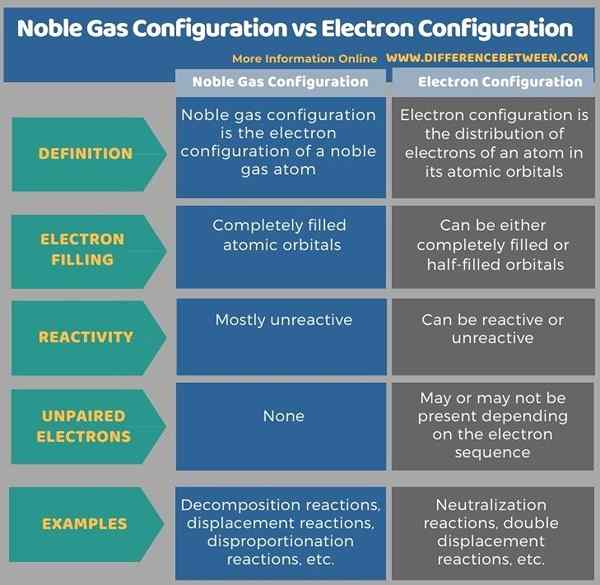
Ringkasan -Konfigurasi Gas Mulia vs Konfigurasi Elektron
Konfigurasi elektron adalah urutan elektron yang terdapat dalam atom. Perbezaan utama antara konfigurasi gas mulia dan konfigurasi elektron adalah bahawa konfigurasi gas mulia hanya mempunyai pasangan elektron manakala konfigurasi elektron boleh mempunyai kedua -dua elektron berpasangan dan tidak berpasangan.
Rujukan:
1. "Gas mulia."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 23 Okt. 2020, boleh didapati di sini.
Ihsan gambar:
1. "Gas Mulia Berkilau" oleh kerja baru Alchemist-hp (bercakap) www.PSE-Mendelejew.de); Imej tunggal asal: Jurii, http: // images-of-elements.com. - Asal: Jurii (CC oleh 3.0) melalui Commons Wikimedia
2. "Orbital Elektron" oleh Patricia.FIDI - Kerja Sendiri oleh Patricia.Fidi dan Lt Paul - Asalnya dari Pl: Grafika: Orbite.PNG, Pengarang PL: Wikipedysta: Chemmix.W3C- (Domain Awam) ini melalui Wikimedia Commons


