Perbezaan antara N2O4 dan NO2
The Perbezaan utama Antara N2O4 dan NO2 ialah N2O4 adalah diamagnet, sedangkan NO2 adalah paramagnetik.
N2O4 adalah dinitrogen tetroksida manakala NO2 adalah nitrogen dioksida. Walaupun formula kimia N2O4 dapat diperoleh dengan menggandakan nilai stoikiometri formula kimia NO2, kedua -dua ini adalah sebatian kimia yang berbeza dengan sifat kimia dan fizikal yang berbeza.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu N2O4
3. Apa itu NO2
4. Perbandingan sampingan - N2O4 vs NO2 dalam bentuk jadual
5. Ringkasan
Apa itu N2O4?
N2O4 adalah dinitrogen tetroksida. Kami biasanya menyebutnya sebagai nitrogen tetroksida. Sebatian ini berlaku sebagai cecair tanpa warna dan merupakan reagen yang sangat berguna dalam proses sintesis kimia. Kompaun ini boleh membentuk campuran keseimbangan dengan nitrogen dioksida. Selanjutnya, dinitrogen tetroksida adalah ejen pengoksidaan yang kuat yang juga hipergolik. Ia adalah hipergolik apabila bersentuhan dengan pelbagai bentuk hidrazin (ini menjadikan campuran hidrazin dan dinitrogen tetroksida bipropel biasa untuk roket).
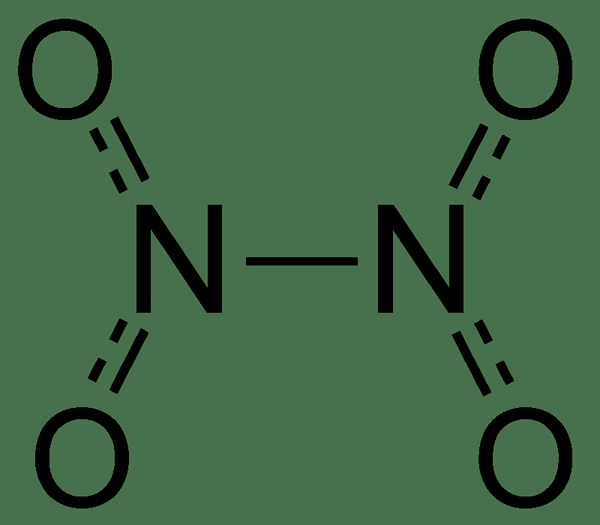
Rajah 01: Pembentukan molekul molekul dinitrogen tetroksida
Kita boleh mempertimbangkan molekul dinitrogen tetroksida sebagai dua kumpulan nitro yang terikat bersama. Dan, tindak balas tertentu ini membentuk campuran keseimbangan dinitrogen tetroksida dan nitrogen dioksida. Juga, kita dapat melihat molekul dinitrogen tetroksida sebagai molekul planar yang mempunyai ikatan lemah antara dua atom nitrogen. Kerana ikatan kimia ini jauh lebih panjang daripada ikatan kimia n-n biasa.
Apabila mempertimbangkan sifat magnet molekul ini, ia adalah diamagnet kerana tidak ada elektron yang tidak berpasangan pada mana -mana atom molekul ini. Selain itu, bahan cecair ini biasanya tidak berwarna, tetapi boleh ada warna kuning juga disebabkan oleh kehadiran NO2 bergantung kepada keseimbangan yang disebutkan di atas. Lebih penting lagi, pada suhu tinggi, keseimbangan menolak ke arah NO2 dan bukannya N2O4.
Dinitrogen tetroksida boleh dihasilkan oleh pengoksidaan pemangkin ammonia, di mana stim digunakan sebagai pencairan untuk mengurangkan suhu pembakaran. Dalam proses tindak balas ini, langkah pertama termasuk pengoksidaan ammonia ke dalam oksida nitrik, dan langkah kedua ialah pengoksidaan nitrik oksida ke dalam nitrogen dioksida, diikuti dengan dimerisasi ke dalam nitrogen tetroksida.
Apa itu NO2?
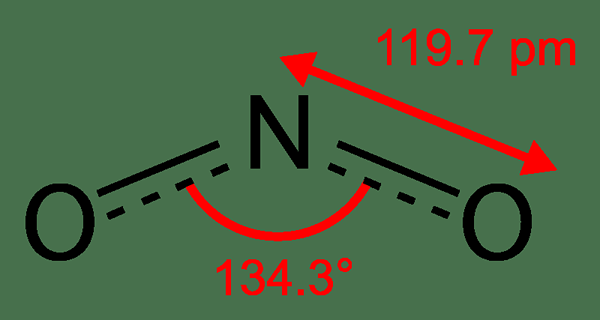
NO2 adalah nitrogen dioksida. Ia adalah salah satu daripada beberapa oksida nitrogen. Kita dapat melihatnya sebagai pertengahan dalam sintesis perindustrian asid nitrik, yang penting dalam pengeluaran baja. Tambahan pula, No2 adalah gas coklat yang mempunyai bau seperti klorin. Apabila ditambah ke air, sebatian ini mengalami hidrolisis. Walau bagaimanapun, bahan gas ini berubah menjadi cecair coklat kekuningan pada suhu rendah. Dan, perubahan warna ini berlaku kerana penukaran NO2 menjadi N2O4.

Rajah 02: Struktur kimia NO2
Secara ciri -ciri, atom nitrogen molekul NO2 mempunyai satu elektron yang tidak berpasangan manakala terdapat dua ikatan n = o dalam molekul. Oleh itu, sebatian ini adalah paramagnet; makna, ia dapat tertarik dengan medan magnet luaran. Selain itu, elektron tunggal yang tidak berpasangan ini juga bermaksud bahawa ia adalah sebatian radikal bebas.
Apabila mempertimbangkan penyediaan bahan NO2, ia biasanya terbentuk melalui pengoksidaan oksida nitrik oleh oksigen di udara. Juga, bahan ini terbentuk dalam kebanyakan proses pembakaran menggunakan udara sebagai ejen pengoksidaan.
Terdapat beberapa kegunaan NO2 yang berbeza, termasuk penggunaannya sebagai pertengahan dalam pembuatan asid nitrik, sebagai ejen nitrat dalam pembuatan bahan letupan kimia, sebagai perencat pempolimeran untuk acrylates, sebagai agen pemutihan tepung, dan lain -lain.
Apakah perbezaan antara N2O4 dan NO2?
N2O4 adalah dinitrogen tetroksida manakala NO2 adalah nitrogen dioksida. Perbezaan utama antara N2O4 dan NO2 ialah N2O4 adalah diamagnet, sedangkan NO2 adalah paramagnetik. Selanjutnya, N2O4 berlaku sebagai cecair, sementara NO2 adalah bahan gas. Selain itu, N2O4 adalah cecair tanpa warna manakala NO2 adalah gas coklat.
Info-grafik berikut menyusun lebih banyak perbezaan antara N2O4 dan NO2 untuk perbandingan sampingan.
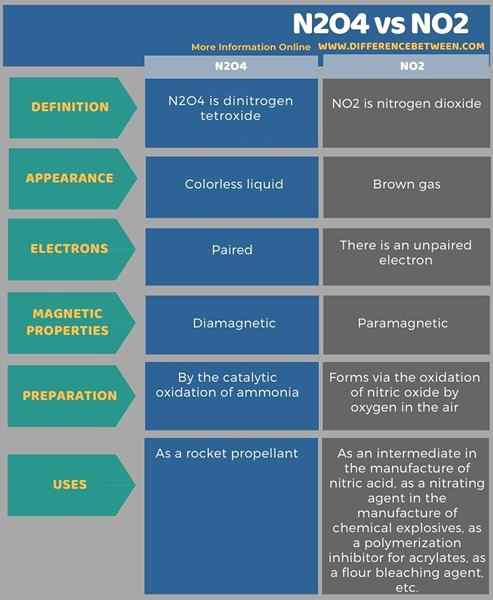
Ringkasan -N2O4 vs NO2
N2O4 adalah dinitrogen tetroksida. NO2 adalah nitrogen dioksida. Apabila mempertimbangkan sifat kimia kedua -dua sebatian ini, sifat magnet sangat penting. Perbezaan utama antara N2O4 dan NO2 ialah N2O4 adalah diamagnet, sedangkan NO2 adalah paramagnetik. Diamagnetic bermaksud molekul N2O4 tidak tertarik dengan medan magnet luaran kerana tidak ada elektron yang tidak berpasangan dalam molekul ini. Paramagnetik bermaksud molekul tertarik kepada medan magnet luaran kerana terdapat elektron yang tidak berpasangan dalam molekul NO2.
Rujukan:
1. "Dinitrogen tetroxide."Pubchem, boleh didapati di sini.
Ihsan gambar:
1. "Dinitrogen Tetroxide" oleh Kemikungen - Kerja Sendiri (Domain Awam) melalui Commons Wikimedia
2. "Nitrogen-dioksida-2d-dimensi-vektor" oleh Zirguezi-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia


