Perbezaan antara undang -undang kadar pembezaan dan undang -undang kadar bersepadu
Perbezaan utama - Undang -undang Kadar Berbeza vs Undang -undang Kadar Bersepadu
Undang -undang kadar pembezaan dan undang -undang kadar bersepadu adalah dua bentuk undang -undang kadar. Perbezaan utama antara undang -undang kadar perbezaan dan undang -undang kadar bersepadu ialah Undang -undang kadar pembezaan memberikan kadar tindak balas kimia sebagai fungsi perubahan kepekatan satu atau lebih reaktan semasa tempoh masa tertentu manakala undang -undang kadar bersepadu memberikan kadar tindak balas kimia sebagai fungsi kepekatan awal satu atau lebih reaktan selepas tempoh masa tertentu.
Kadar tindak balas adalah ukuran perubahan kepekatan reaktan atau produk semasa perkembangan tindak balas kimia. Undang -undang kadar yang berbeza digunakan untuk menjelaskan kemajuan reaksi. Undang -undang kadar ini dinyatakan sebagai hubungan matematik antara parameter yang berbeza.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah undang -undang kadar perbezaan
3. Apakah undang -undang kadar bersepadu
4. Hubungan antara undang -undang kadar pembezaan dan undang -undang kadar bersepadu
5. Perbandingan sampingan - Undang -undang kadar pembezaan vs undang -undang kadar bersepadu dalam bentuk jadual
6. Ringkasan
Apakah undang -undang kadar perbezaan?
Undang -undang kadar pembezaan digunakan untuk menentukan kadar tindak balas kimia sebagai fungsi perubahan kepekatan satu atau lebih reaktan dalam tempoh masa tertentu. Undang -undang kadar pembezaan menunjukkan apa yang berlaku pada tahap molekul tindak balas kimia. Mekanisme keseluruhan tindak balas kimia dapat ditentukan menggunakan undang -undang kadar pembezaan (penukaran reaktan ke dalam produk).
Persamaan undang -undang kadar pembezaan
Undang -undang kadar pembezaan untuk tindak balas kimia di bawah boleh diberikan sebagai ungkapan matematik.
A → B + C
Kadar = - d [a] / dt = k [a]n
Di sini, [A] adalah kepekatan reaktan "a" dan "k" adalah kadar pemalar. "N" memberikan urutan reaksi. Persamaan undang -undang kadar pembezaan boleh diintegrasikan untuk mendapatkan hubungan yang jelas antara [a] dan masa "t". Integrasi ini memberikan undang -undang kadar bersepadu.

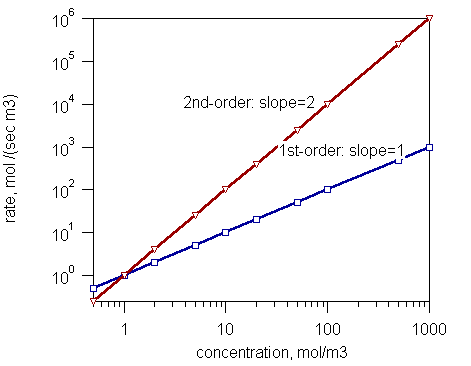
Rajah 1: Graf yang menunjukkan susunan tindak balas
Apakah undang -undang kadar bersepadu?
Undang -undang kadar bersepadu memberikan kadar tindak balas kimia sebagai fungsi kepekatan awal satu atau lebih reaktan selepas tempoh tertentu. Undang -undang kadar bersepadu boleh digunakan untuk menentukan kadar pemalar tindak balas kimia tertentu, dan susunan tindak balas dapat diperolehi melalui data eksperimen.
Persamaan undang -undang kadar bersepadu
Untuk tindak balas kimia A → B + C, undang -undang kadar bersepadu boleh dinyatakan sebagai ungkapan matematik seperti yang diberikan di bawah.
ln [a] = -kt + ln [a]0
Di sini, [a]0 adalah kepekatan awal reaktan A dan [A] adalah kepekatan reaktan "A" selepas masa "T" telah berlalu. Walau bagaimanapun, undang -undang kadar bersepadu berbeza antara satu sama lain berdasarkan susunan tindak balas "n". Persamaan di atas diberikan untuk tindak balas kimia pesanan sifar.
Untuk Reaksi pesanan pertama, persamaan undang -undang kadar adalah,
[A] = [a] e-kt
Untuk tindak balas pesanan kedua, persamaan undang -undang kadar adalah,
1/[a] = 1/[a]0 + kt
Untuk menentukan Nilai pemalar tindak balas, persamaan di atas boleh digunakan seperti berikut.
Untuk tindak balas pesanan pertama,
k = ln [a] - ln [a]0 / t
Untuk tindak balas pesanan kedua,
k = 1/[a] - 1/[a]0 / t
Apakah hubungan antara undang -undang kadar pembezaan dan undang -undang kadar bersepadu?
- Undang -undang kadar pembezaan tindak balas kimia dapat diintegrasikan untuk mendapatkan undang -undang kadar bersepadu tindak balas kimia yang sama.
Apakah perbezaan antara undang -undang kadar pembezaan dan undang -undang kadar bersepadu?
Undang -undang Kadar Berbeza vs Undang -undang Kadar Bersepadu | |
| Undang -undang kadar pembezaan digunakan untuk menentukan kadar tindak balas kimia sebagai fungsi perubahan kepekatan satu atau lebih reaktan dalam tempoh masa tertentu. | Undang -undang kadar bersepadu memberikan kadar tindak balas kimia sebagai fungsi kepekatan awal (atau kepekatan pada saat tertentu) satu atau lebih reaktan selepas tempoh tertentu. |
| Permohonan | |
| Undang -undang kadar pembezaan boleh digunakan untuk menunjukkan apa yang berlaku di tahap molekul tindak balas kimia dan, mekanisme keseluruhan tindak balas kimia dapat ditentukan menggunakan undang -undang kadar ini. | Undang -undang kadar bersepadu boleh digunakan untuk menentukan kadar pemalar tindak balas kimia tertentu. |
| Penggunaan | |
| Undang -undang kadar pembezaan sukar digunakan apabila dibandingkan dengan undang -undang kadar bersepadu. | Undang -undang bersepadu menjadikannya mudah untuk menentukan hubungan yang jelas antara kepekatan reaktan dan masa berlalu. |
Ringkasan -Undang -undang Kadar Berbeza vs Undang -undang Kadar Bersepadu
Menilai undang -undang tindak balas kimia memberikan hubungan antara kadar tindak balas dan kepekatan reaktan. Perbezaan utama antara undang -undang kadar pembezaan dan undang -undang kadar bersepadu ialah undang -undang kadar pembezaan memberikan kadar tindak balas kimia sebagai fungsi perubahan kepekatan satu atau lebih reaktan semasa tempoh masa tertentu manakala undang -undang kadar bersepadu memberikan kadar tindak balas kimia sebagai fungsi kepekatan awal satu atau lebih reaktan selepas tempoh tertentu.
Rujukan:
1. "Kadar undang -undang - perbezaan."Kimia Libretexts, Libretexts, 17 Julai 2015, boleh didapati di sini.
2. Libretexts. "12.4: Undang -undang Kadar Bersepadu."Kimia Libretexts, Libretexts, 11 Sept. 2017, boleh didapati di sini.]
Ihsan gambar:
1. "Rateloglogplot" oleh Fabiuccio ~ Enwikibooks di Wikibooks Bahasa Inggeris - dipindahkan dari en.Wikibooks ke Commons.(Domain Awam) melalui Wikimedia Commons


