Perbezaan antara deuterium dan tritium
The Perbezaan utama antara deuterium dan tritium ialah Nukleus Deuterium mempunyai satu neutron manakala tritium nukleus mempunyai dua neutron.
Hidrogen adalah elemen pertama dan terkecil dalam jadual berkala, yang kami nyatakan sebagai h. Ia mempunyai satu elektron dan satu proton. Kita boleh mengkategorikannya di bawah kumpulan 1 dan tempoh 1 dalam jadual berkala kerana konfigurasi elektronnya: 1S1. Hidrogen boleh mengambil elektron untuk membentuk ion yang dikenakan negatif, atau dengan mudah boleh mendermakan elektron untuk menghasilkan proton yang dikenakan positif. Jika tidak, ia boleh berkongsi elektron untuk membuat bon kovalen. Kerana keupayaan ini, hidrogen hadir dalam sejumlah besar molekul, dan ia adalah unsur yang sangat banyak di bumi. Hidrogen mempunyai tiga isotop sebagai protium-1H (tiada neutron), deuterium-2h (satu neutron) dan tritium-3H (dua neutron). Protium adalah yang paling banyak di antara ketiga -tiga mereka, mempunyai kira -kira 99% kelimpahan relatif.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu deuterium
3. Apa itu tritium
4. Perbandingan sampingan - Deuterium vs tritium dalam bentuk jadual
5. Ringkasan
Apa itu deuterium?
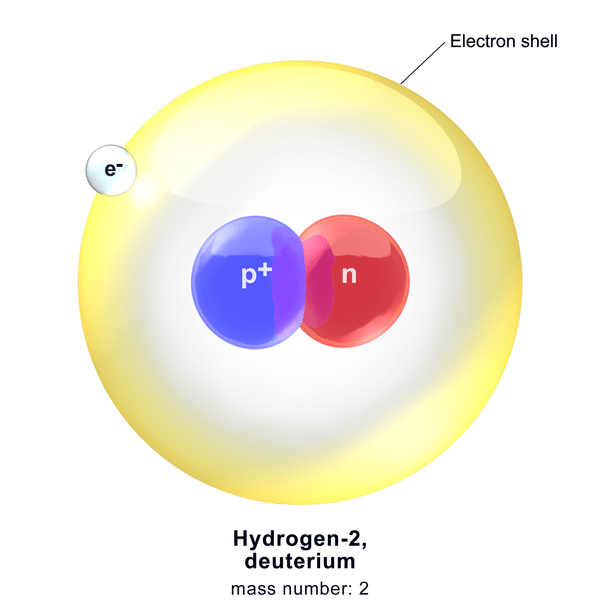
Deuterium adalah salah satu isotop hidrogen. Ia adalah isotop yang stabil dengan 0.015% kelimpahan semula jadi. Terdapat proton dan neutron dalam nukleus deuterium. Oleh itu, bilangan jisimnya adalah dua, dan nombor atom adalah satu. Kami memanggil isotop ini sebagai hidrogen berat dan ditunjukkan sebagai 2h. Walau bagaimanapun, yang paling biasa, kami mewakilinya dengan D.

Rajah 1: Deuterium
Deuterium boleh wujud sebagai molekul gas diatomik dengan formula kimia d2. Walau bagaimanapun, kemungkinan menyertai dua atom D dalam alam adalah rendah disebabkan oleh kelimpahan yang lebih rendah. Oleh itu, isotop ini kebanyakannya mengikat dengan atom 1H yang membuat gas -HD (hidrogen deuteride). Juga, dua atom deuterium boleh mengikat dengan oksigen untuk membentuk air analog D2O, yang kami panggil air berat.
Selain itu, molekul dengan deuterium menunjukkan sifat kimia dan fizikal yang berbeza daripada analog hidrogen mereka. Contohnya, ia dapat mempamerkan kesan isotop kinetik. Tambahan pula, sebatian deuterated menunjukkan perbezaan ciri dalam NMR, IR dan spektroskopi massa; Oleh itu, kita dapat mengenalinya menggunakan kaedah tersebut. Juga, deuterium mempunyai putaran satu. Oleh itu, di NMR, gandingan isotop ini memberikan triplet. Selain itu, ia menyerap kekerapan IR yang berbeza daripada hidrogen dalam spektroskopi IR. Oleh kerana perbezaan besar -besaran, dalam spektroskopi massa, deuterium boleh dibezakan dari hidrogen.
Apa itu tritium?
Tritium adalah isotop hidrogen yang nombor jisimnya adalah tiga. Oleh itu, nukleus tritium mempunyai satu proton dan dua neutron. Ia hanya wujud dalam jumlah jejak kerana radioaktiviti. Kerana sebab ini, ia harus dihasilkan secara buatan untuk penggunaan praktikal.
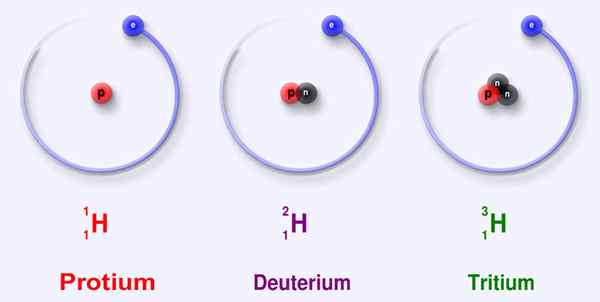
Rajah 02: Tiga isotop utama hidrogen
Tritium adalah isotop radioaktif (ini adalah satu -satunya isotop radioaktif hidrogen). Ia mempunyai separuh hayat 12 tahun, dan ia merosot dengan memancarkan zarah beta untuk menghasilkan helium-3. Jisim atom isotop ini adalah 3.0160492. Selain itu, ia wujud sebagai gas (HT) pada suhu dan tekanan standard. Juga, ia boleh membentuk oksida (HTO), yang kami panggil "air yang tritiated."Tritium berguna dalam membuat senjata nuklear dan sebagai pengesan dalam kajian biologi dan alam sekitar.
Apakah perbezaan antara deuterium dan tritium?
Deuterium dan tritium adalah dua isotop hidrogen. Perbezaan utama antara deuterium dan tritium ialah nukleus deuterium mempunyai satu neutron manakala nukleus tritium mempunyai dua neutron. Tambahan pula, jumlah deuterium adalah 2.0135532 manakala jumlah tritium jisim adalah 3.0160492. Jadi, ini adalah satu lagi perbezaan yang signifikan antara deuterium dan tritium.
Selain itu, perbezaan selanjutnya antara deuterium dan tritium adalah bahawa deuterium adalah isotop yang stabil dan kita dapat menemuinya sedangkan tritium adalah isotop radioaktif yang kita tidak dapat menemuinya. Walau bagaimanapun, kita boleh menghasilkannya secara buatan untuk penggunaan praktikal.

Ringkasan -Deuterium vs Tritium
Deuterium dan tritium adalah isotop hidrogen elemen kimia. Perbezaan utama antara deuterium dan tritium ialah nukleus deuterium mempunyai satu neutron manakala nukleus tritium mempunyai dua neutron. Selain itu, tritium adalah radioaktif manakala deuterium adalah isotop yang stabil.
Rujukan:
1. Helmenstine, Anne Marie, PH.D. "Fakta deuterium."Thoughtco, APR. 2, 2019, boleh didapati di sini.
Ihsan gambar:
1. "Blausen 0527 Hydrogen -2 Deuterium" oleh Bruceblaus - Kerja Sendiri (CC oleh 3.0) melalui Commons Wikimedia
2. "Protium Deuterium Tritium" oleh Lamiot untuk versi Perancis, dari Dirk Hünniger - diri, terjemahan dari Dirk Hünniger (Wikipedia Jerman) (CC By -SA 3.0) melalui Commons Wikimedia


