Perbezaan antara klorida dan klorat
The Perbezaan utama antara klorida dan klorat ialah Anion klorida mengandungi hanya satu atom manakala anion klorat mengandungi empat atom. Tambahan pula, keadaan pengoksidaan klorin dalam anion klorida adalah -1, dan dalam anion klorat, ia adalah +5.
Kedua -dua klorida dan klorat adalah anion klorin. Klorin adalah elemen kimia yang mempunyai nombor atom 17. Menurut konfigurasi elektronnya, terdapat elektron yang tidak berpasangan di orbital P yang paling luarnya. Elektron yang tidak berpasangan ini menjadikan klorin sangat reaktif. Ia membentuk pelbagai anion termasuk klorida dan klorat. Marilah kita bercakap lebih lanjut mengenai mereka.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu klorida
3. Apa itu klorat
4. Persamaan antara klorida dan klorat
5. Perbandingan sampingan - klorida vs klorat dalam bentuk jadual
6. Ringkasan
Apa itu klorida?
Klorida adalah anion klorin yang mempunyai formula kimia cl-. Menurut konfigurasi elektron atom klorin, ia mempunyai elektron yang tidak berpasangan di orbital P. Oleh itu, ia cenderung mendapatkan elektron dari luar untuk menyelesaikan elektronnya. Elektron masuk ini mempunyai caj negatif. Oleh itu, ia memberikan atom klorin sebagai caj negatif tambahan dan membentuk ion klorida.
Jisim molar anion ini ialah 35.5 g/mol. Ia sama dengan jisim molar atom klorin kerana jisim elektron boleh diabaikan apabila kita membandingkannya dengan massa neutron dan proton. Walau bagaimanapun, anion ini lebih besar daripada atom klorin. Selain itu, ia adalah diamagnet. Sebilangan besar sebatian yang mengandungi anion ini sangat larut dalam air. Apabila mempertimbangkan berlakunya anion ini, air laut mengandungi sekitar 1.94% ion klorida.
Apa itu klorat?
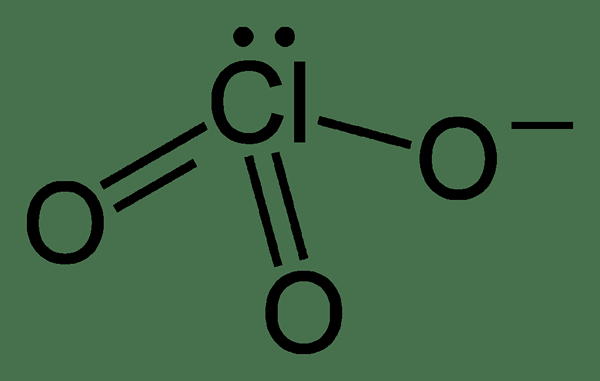
Klorat adalah anion klorin yang mempunyai formula kimia CLO-3. Anion ini mempunyai satu atom klorin yang terikat kepada tiga atom oksigen; dua ikatan cl = o dan satu ikatan cl-o. Di samping itu, anion ini mempunyai pasangan elektron tunggal pada atom klorin. Oleh kerana struktur ini, anion ini mempunyai pelbagai struktur resonans. Oleh itu, atom klorin berada dalam keadaan pengoksidaan +5 di sini. Geometri anion ini adalah geometri piramid trigonal.

Rajah 02: Struktur kimia ion klorat
Spesies kimia ini bertindak sebagai pengoksida yang kuat. Ini bermaksud bahawa ia dapat mengoksidakan bahan lain dengan mudah sambil mengurangkan dirinya. Kita dapat menghasilkan sebatian yang mengandungi ion -ion ini di makmal. Sebagai contoh, tindak balas antara gas klorin dan KOH panas membentuk kalium klorat (KCLO3). Walau bagaimanapun, kejadian semula jadi sebatian ini belum disahkan. Selain itu, sebatian yang mengandungi anion ini agak toksik.
Apakah persamaan antara klorida dan klorat?
- Kedua -duanya adalah anion
- Kedua -duanya membawa caj elektrik bersih -1
- Klorida dan klorat adalah derivatif klorin
Apakah perbezaan antara klorida dan klorat?
Klorida adalah anion klorin yang mempunyai formula kimia cl-. Ia mempunyai satu atom. Jisim molar ion ini ialah 35.5 g/mol. Selanjutnya, keadaan pengoksidaan klorin dalam ion ini ialah -1. Klorat adalah anion klorin yang mempunyai formula kimia CLO-3. Ia mempunyai empat atom. Ini adalah perbezaan utama antara klorida dan klorat. Selain itu, jisim molar klorat adalah 83.4 g/mol. Di samping itu, keadaan pengoksidaan klorin dalam ion ini ialah +5.

Ringkasan -klorida vs klorat
Kedua -dua klorida dan klorat adalah anion yang berasal dari klorin. Perbezaan antara klorida dan klorat ialah anion klorida mengandungi hanya satu atom manakala anion klorat mengandungi empat atom. Juga, keadaan pengoksidaan klorin dalam anion klorida adalah -1, dan dalam anion klorat, ia adalah +5.
Rujukan:
1. "Klorida."Wikipedia, Yayasan Wikimedia, 23 Julai 2018. Terdapat di sini
2. "Klorat."Wikipedia, Yayasan Wikimedia, 15 Julai 2018. Terdapat di sini
Ihsan gambar:
1.'Cl -'by Neurotiker - Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia
2.'Chlorate-2d'by Benjah-bmm27-kerja sendiri, (domain awam) melalui Commons Wikimedia


