Perbezaan antara benzena dan sikloheksana
The Perbezaan utama antara benzena dan sikloheksana ialah benzena adalah sebatian aromatik manakala sikloheksana adalah sebatian bukan aromatik.
Saintis, Kekule mendapati struktur benzena pada tahun 1872. Kerana aromatik, benzena berbeza dari sebatian alifatik yang lain. Oleh itu, ia adalah bidang pengajian yang berasingan dalam kimia organik. Sebaliknya, walaupun sikloheksana mempunyai bentuk yang sama dengan benzena, ia tidak aromatik. Cyclohexane adalah alkana tepu, yang mempunyai sifat yang berbeza daripada benzena.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu benzena
3. Apa itu sikloheksana
4. Perbandingan sampingan - benzena vs sikloheksana dalam bentuk tabular
5. Ringkasan
Apa itu benzena?
Benzene hanya mempunyai atom karbon dan hidrogen yang diatur untuk memberikan struktur planar. Ia mempunyai formula molekul c6H6. Strukturnya dan beberapa sifat penting adalah seperti berikut.
- Benzene adalah cecair tanpa warna dengan bau manis.
- Ia mudah terbakar dan menyejat dengan cepat apabila terdedah.
- Berguna sebagai pelarut, kerana ia dapat membubarkan banyak sebatian bukan polar.
- Ia sedikit larut dalam air.
- Penghapusan elektron PI.
Struktur benzena
Struktur benzena adalah unik berbanding dengan hidrokarbon alifatik yang lain. Oleh itu, benzena mempunyai sifat unik. Semua karbon di benzena mempunyai tiga sp2 orbital hibrid. Dua sp2 Orbital hibrida karbon bertindih dengan SP2 orbital hibrida karbon bersebelahan di kedua -dua belah pihak. Sp2 tumpang tindih orbit hibrid dengan orbital hidrogen untuk membentuk ikatan σ.
Juga, elektron dalam orbital p tumpang tindih karbon dengan elektron P atom karbon di kedua -dua belah pihak membentuk ikatan PI. Tumpahan elektron ini berlaku di semua enam atom karbon dan, oleh itu, menghasilkan sistem ikatan Pi, yang tersebar di seluruh cincin karbon. Oleh itu, kita mengatakan bahawa elektron -elektron ini menjadi diselaraskan. Penyingkiran elektron bermaksud bahawa tidak ada ikatan berganda dan tunggal bergantian. Oleh itu, semua panjang ikatan C-C adalah sama, dan panjangnya antara panjang ikatan tunggal dan berganda. Hasil daripada penyahkawalan, cincin benzena stabil, oleh itu, enggan menjalani tindak balas tambahan, tidak seperti alkenes lain.
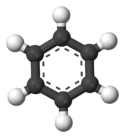
Rajah 01: Model tongkat dan bola untuk benzena
Sumber benzena termasuk produk semula jadi atau pelbagai bahan kimia yang disintesis. Sememangnya, ia berlaku dalam petrokimia seperti minyak mentah atau petrol. Mengenai produk sintetik, benzena hadir dalam beberapa plastik, pelincir, pewarna, getah sintetik, detergen, ubat, asap rokok dan racun perosak. Benzene dibebaskan pada pembakaran bahan di atas. Oleh itu, ekzos kereta dan pelepasan kilang juga mengandungi benzena. Di atas semua, ia adalah karsinogenik, jadi pendedahan kepada tahap benzena yang tinggi boleh menyebabkan kanser.
Apa itu sikloheksana?
Cyclohexane adalah molekul siklik dengan formula c6H12. Walaupun ia mempunyai bilangan karbon yang sama seperti benzena, sikloheksana adalah molekul tepu. Oleh itu, tidak ada ikatan berganda antara karbon seperti dalam benzena. Juga, ia adalah cecair yang tidak berwarna dengan bau manis yang ringan.

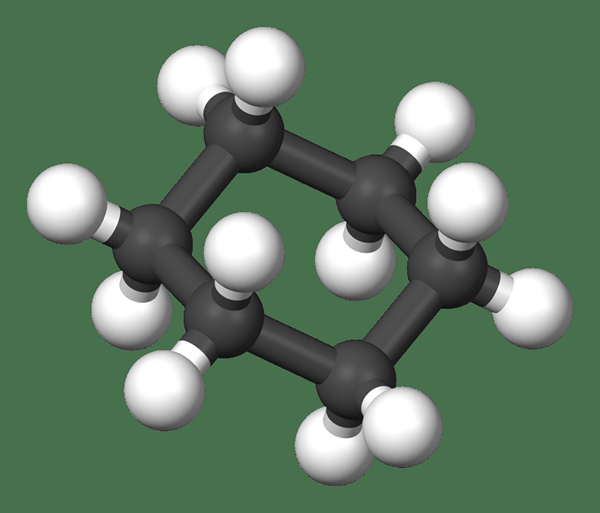
Rajah 02: Model bola dan tongkat untuk sikloheksana
Tambahan pula, kita dapat menghasilkan sebatian ini melalui tindak balas antara benzena dan hidrogen. Oleh kerana ini adalah sikloalkane, ia agak tidak aktif. Juga, ia adalah nonpolar dan hidrofobik. Oleh itu, ini berguna sebagai pelarut nonpolar dalam aplikasi makmal. Selain itu, sikloheksana adalah salah satu sikloalkane yang paling stabil, kerana ketegangan cincinnya adalah minimum. Oleh itu, ia menghasilkan sedikit haba apabila terbakar berbanding dengan sikloalkan lain.
Apakah perbezaan antara benzena dan sikloheksana?
Benzene adalah sebatian organik yang mempunyai formula kimia c6H6 dan struktur planar manakala sikloheksana adalah molekul siklik dengan formula c6H12. Perbezaan utama antara benzena dan sikloheksana ialah benzena adalah sebatian aromatik manakala sikloheksana adalah sebatian bukan aromatik. Ini kerana, tidak ada ikatan berganda antara atom karbon dalam cincin sikloheksana. Satu lagi perbezaan penting antara benzena dan sikloheksana ialah benzena adalah molekul tak tepu manakala sikloheksana adalah molekul tepu. Kerana benzena mempunyai atom karbon di gelanggang dengan SP2 hibridisasi manakala sikloheksana mempunyai atom karbon di cincin dengan SP3 Hibridisasi.
Infographic di bawah perbezaan antara benzena dan sikloheksana menunjukkan lebih banyak perbezaan antara kedua -dua.

Ringkasan -Benzene vs Cyclohexane
Benzena dan sikloheksana kedua-dua struktur cincin enam anggota. Tetapi mereka berbeza antara satu sama lain mengikut ikatan kimia antara atom karbon; Oleh itu, geometri molekul. Oleh kerana ikatan antara atom karbon menentukan aromatik molekul, kita dapat menekankan bahawa perbezaan utama antara benzena dan sikloheksana sebagai; Benzene adalah sebatian aromatik manakala sikloheksana adalah sebatian bukan aromatik.
Rujukan:
1. "Benzene."Wikipedia, Yayasan Wikimedia, 27 Sept. 2018. Terdapat di sini
2. "Cyclohexane."Wikipedia, Yayasan Wikimedia, 10 Okt. 2018. Terdapat di sini
Ihsan gambar:
1."Benzene-Aromatic-3D-Balls" oleh Benjah-Bmm27-Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia
2."Cyclohexane-Chair-3D-Balls" (Domain Awam) melalui Commons Wikimedia


