Perbezaan antara aktiviti dan fugacity
The Perbezaan utama antara aktiviti dan fugacity adalah Aktiviti merujuk kepada kepekatan spesies kimia yang berkesan di bawah keadaan yang tidak sesuai, sedangkan fugacity merujuk kepada tekanan separa yang berkesan bagi spesies kimia di bawah keadaan yang tidak ideal.
Aktiviti dan fugacity adalah konsep kimia penting dalam termodinamik. Terma ini ditakrifkan untuk tingkah laku bukan ideal gas sebenar.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu aktiviti
3. Apa itu Fugacity
4. Perbandingan sampingan - Aktiviti vs Fugacity dalam bentuk jadual
5. Ringkasan
Apa itu aktiviti?
Aktiviti adalah ukuran kepekatan spesies kimia yang berkesan di bawah tingkah laku yang tidak sesuai. Konsep aktiviti dirancang oleh ahli kimia Amerika Gilbert n. Lewis. Aktiviti adalah kuantiti tanpa dimensi. Nilai aktiviti untuk sebatian tertentu bergantung pada keadaan standard spesies tersebut. Sebagai contoh, nilai bahan dalam fasa pepejal atau cecair diambil sebagai 1. Bagi gas, aktiviti merujuk kepada tekanan separa yang berkesan, iaitu fugacity/tekanan gas yang kita anggap. Selain itu, aktiviti bergantung kepada faktor berikut:
- Suhu
- Tekanan
- Komposisi campuran, dll.
Maksudnya; Sekitar mempengaruhi aktiviti spesies kimia. Molekul gas di bawah keadaan tidak ideal cenderung berinteraksi antara satu sama lain, sama ada menarik atau menangkis antara satu sama lain. Oleh itu, aktiviti molekul atau ion dipengaruhi oleh spesies kimia yang terdapat di sekitarnya.
Apa itu Fugacity?
Fugacity adalah ukuran tekanan separa berkesan spesies kimia di bawah keadaan yang tidak ideal. Nilai fugacity untuk spesies kimia tertentu seperti gas sebenar adalah sama dengan tekanan gas ideal yang mempunyai tenaga dan tenaga gibbs molar sama dengan gas sebenar. Kita dapat menentukan fugacity menggunakan kaedah eksperimen atau menggunakan beberapa model lain seperti gas van der waals (yang lebih dekat dengan gas sebenar dan bukannya gas yang ideal).
Koefisien Fugacity adalah hubungan antara tekanan gas sebenar dan fugacitynya. Kita boleh menunjukkannya menggunakan simbol φ. Hubungannya,
φ = f/p
Di sini, f adalah fugacity, sementara p adalah tekanan gas sebenar. Untuk gas yang ideal, nilai tekanan dan fugacity adalah sama. Oleh itu, pekali fugacity untuk gas ideal adalah 1.

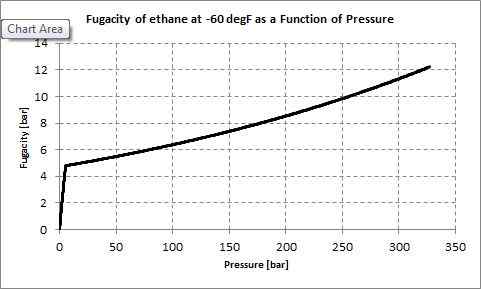
Rajah 01: Fugacity of Ethane
Selain itu, konsep fugacity ini berkait rapat dengan aktiviti atau aktiviti termodinamik. Kita boleh memberikan hubungan ini, aktiviti = fugacity/tekanan.
Apakah perbezaan antara aktiviti dan fugacity?
Perbezaan utama antara aktiviti dan fugacity ialah aktiviti merujuk kepada kepekatan spesies kimia yang berkesan di bawah keadaan yang tidak ideal, sedangkan fugacity merujuk kepada tekanan separa yang berkesan dari spesies kimia di bawah keadaan yang tidak sesuai. Oleh itu, dalam konsep, aktiviti termodinamik adalah kepekatan molekul sebenar yang berkesan, i.e. Gas sebenar, sementara Fugacity adalah tekanan separa yang berkesan dari gas sebenar. Selain itu, kita dapat menentukan fugacity menggunakan kaedah eksperimen atau menggunakan beberapa model lain seperti gas van der Waals (yang lebih dekat dengan gas sebenar dan bukannya gas yang ideal), dan nilai ini sama dengan aktiviti*tekanan gas sebenar.
Di bawah infographic meringkaskan perbezaan antara aktiviti dan fugacity.
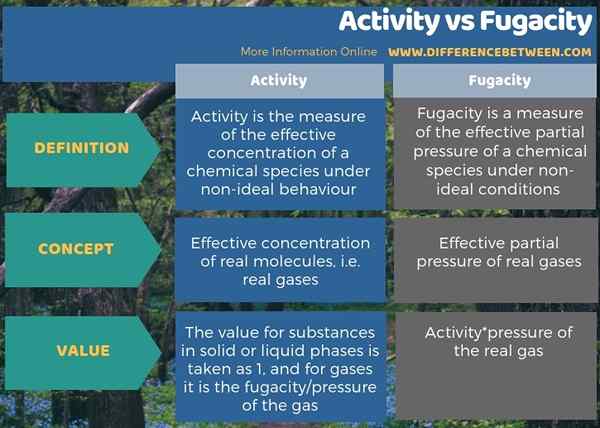
Ringkasan -Aktiviti vs Fugacity
Aktiviti dan fugacity adalah konsep kimia penting dalam termodinamik. Ringkas.
Rujukan:
1. Jones, Andrew Zimmerman. "Undang -undang termodinamik."Pemikiran, Sep. 7, 2019, boleh didapati di sini.
Ihsan gambar:
1. "Fugacity berbanding tekanan etana pada -60 degf" oleh Stieltjes -Grafik Excel menggunakan Peng -Robinson EOS (CC BY -SA 3.0) melalui Commons Wikimedia


